Le rapport albumine/créatinine urinaire (RAC), sur un échantillon du premier matin, guide la prévention cardio‑rénale et complète le DFGe pour détecter précocement le risque cardio‑rénal. Le RAC, catégorisé de A1 à A3, prédit les événements rénaux et cardiovasculaires sans seuil et sert de cible thérapeutique. Toute anomalie doit se confirmer par deux mesures à 3–6 mois. En France, l'examen est disponible, remboursé et doit figurer dans un compte rendu standardisé en mg/g. En soins primaires, il faut associer un contrôle tensionnel IEC/ARA2, iSGLT2/ARM selon les indications et viser une baisse du RAC ≥ 30 % pour les catégories A2/A3.
CE QUE NOUS FAISONS (AUJOURD’HUI)
Mesurer et confirmer
Demander un RAC urinaire sur premier matin, exprimé en mg/g. En cas d'anomalie, confirmer par deux mesures supplémentaires à 3–6 mois, hors exercice, fièvre, poussée tensionnelle ou hyperglycémie. Les bandelettes ne dépistent pas de manière fiable.
Classer et stratifier le risque
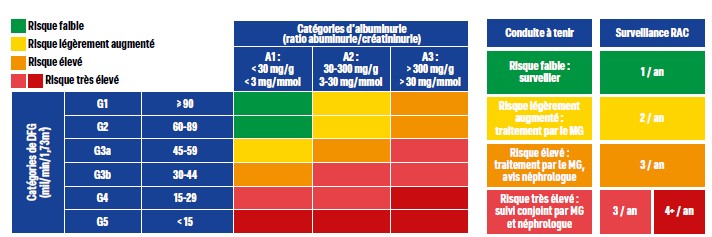
La classification internationale KDIGO distingue trois catégories d’albuminurie : A1(>30mg/g), A2(30—300mg/g), A3 (>300mg/g) – A2 correspond à la «microalbuminurie», terme obsolète. Le risque rénal et cardiovasculaire s'accroît de façon continue avec le RAC, sans seuil1,3. La matrice GA (DFG et albuminurie) résume les indications pour la surveillance et les indications thérapeutiques (Figure 1).
Qui dépister ?
Le RAC doit être mesuré chez de nombreuses catégories de patients :.
- Diabète de type 1 ou 2, mesure annuelle du RAC et du DFGe ;
- Hypertension, dosage au diagnostic, puis tous les cinq ans si normal ;
- Dépistage ciblé après 60 ans et en cas d’obésité, de maladie cardiovasculaire, d’antécédents familiaux de maladie rénale ou de traitement néphrotoxique1,2.
Comment l’interpréter ?
Un RAC < 30 mg/g rassure, sans éliminer un risque cardiovasculaire si d’autres facteurs s’additionnent. Un RAC 30–300mg/g (A2) persistant signe une atteinte glomérulaire et impose une intensification thérapeutique.
Figure 1 : Matrice GA pour stratifier le risque de progression de la maladie rénale chronique et de morbi-mortalité cardiovasculaire (d'après HAS,2023 et KDIGO, 2024). MRC, maladie rénale chronique ; CV, cardiovasculaire ; DFGe, débit de filtration glomérulaire estimé.
Surveillance du traitement par iSGLT2 d’une maladie rénale chronique
Quand recontrôler et quel délai d’effet attendu ?
- RAC. Le contrôle 3 mois après initiation permet de juger de l’effet stabilisé. La baisse d’albuminurie est détectable dès 1 mois, souvent maximale vers 3 mois. L’amplitude moyenne est de −20 % à −30 %, variable selon le niveau de base.
- DFGe. On peut accepter un décrochage initial de 10–20 % ; une baisse > 30 % doit conduire à une évaluation (AINS, surdosage diurétique). Il n’y a pas d’obligation de contrôle très rapproché si le patient est stable, mais plus rapproché en cas de fragilité, traitement diurétique, hypotension ou symptômes. Surveillance et prévention des effets indésirables
Il n’y a pas d’obligation de contrôle très rapproché si le patient est stable, mais plus rapproché en cas de fragilité, traitement diurétique, hypotension ou symptômes.
Surveillance et prévention des effets indésirables
- Péri-opératoire et maladies aiguës : arrêter 3 jours avant une chirurgie programmée ; appliquer des « sick day rules » en cas de jeûne, vomissements/diarrhées, infection sévère ; reprise du traitement après hydratation et rétablissement de l’alimentation.
- Acidocétose euglycémique : rare ; risque accru en cas d’insulinopénie, de régime cétogène, de sevrage alimentaire, de contexte péri-opératoire. Informer des signes d’alerte (nausées, vomissements, douleurs abdominales, soif excessive, dyspnée, confusion, fatigue inhabituelle ou somnolence).
- Infections génitales mycosiques : fréquentes, généralement bénignes ; elles nécessitent une hygiène locale et un traitement antifongique, et n’empêchent pas la poursuite de l'iSGLT2.
- Hypovolémie/hypotension : surveiller la PA et la volémie, ajuster les diurétiques si nécessaire ; prudence chez le sujet âgé.
- Hypoglycémie : surtout en association avec l’insuline ou les sulfamides ; envisager un ajustement des posologies.
- NB : les iSGLT2 n’augmentent pas le risque d’infection urinaire et peuvent être poursuivis. Une étude récente a montré une surmortalité de 30 % lorsque les iSGLT2 sont arrêtés à tort pour cette raison, sans réduction du risque de récidive d’infection urinaire.
Un RAC > 300mg/g(A3) persistant traduit une maladie rénale établie et un risque cardio-rénal élevé, indépendamment du DFGe1-4. Sur le plan physiopathologique, l’augmentation du RAC reflète une dysfonction endothéliale diffuse et une hypertension intra-glomérulaire.
La persistance d’une albuminurie élevée participe à la progression de la maladie rénale par des mécanismes inflammatoires et fibrosants tubulo-interstitiels.
Conduite à tenir en première ligne
L’objectif est double : réduire le risque cardio-rénal et ralentir le déclin rénal.
- Cibler une pression artérielle systolique <130 voire 120mmHg, si tolérée1.
- Optimiser le blocage du SRAA par IEC ou ARA2 en A2/A3, titrés à la dose maximale tolérée1,2.
- Introduire un inhibiteur de SGLT2 en cas de diabète ou de maladie rénale chronique (MRC) albuminurique, la baisse moyenne du RAC est de l’ordre de 20 à 30%, parallèle à la réduction d’événements rénaux1,2. Pour les détails du suivi cf. encadré ci-contre.
- Viser la valeur d’albuminurie la plus basse possible ; une réduction ≥30% du RAC constitue une cible pragmatique reconnue comme substitut pertinent d’événements rénaux dans le diabète1,2,5.
- Surveiller la kaliémie 1 à 2 semaines après chaque introduction ou titration d’un IEC/ARA2, pour maintenir les traitements protecteurs en corrigeant la dyskaliémie plutôt qu’en les interrompant 1,2.
Pièges de laboratoire et d’interprétation
Privilégier l'échantillon du premier matin, mieux corrélé au recueil de 24 h qu'une miction aléatoire. Les laboratoires tendent à exprimer le RAC en mg/g, ce qui évite la confusion avec les mg/mmol. Le RAC peut varier avec la créatininurie ; une faible masse musculaire ou certaines habitudes alimentaires modifient la valeur de référence, d'où l'intérêt du premier matin et de mesures répétées. Les bandelettes restent inadaptées au dépistage d'une élévation modérée1,6.
Aspects pratiques et remboursement en France
Le RAC sur échantillon est simple, disponible en ville et peu coûteux. Il est recommandé et remboursé dans le diabète, l'hypertension et la MRC2,7. Les recommandations de la HAS de 2023 plaident pour des comptes rendus standardisés : expression en mg/g, rappel de la nécessité de confirmation en cas d'anomalie et ajout d'aides à la décision comme la matrice GA ou le score KFRE (score de risque rénal) si c'est pertinent2.
Quand adresser au néphrologue ?
Il faut adresser à un néphrologue si l'une de ces situations est présente :
- RAC > 300 mg/g(A3) ;
- DFGe < 45 ml/min/1,73 m² ;
- Déclin rapide du DFGe>5 ml/min/1,73 m²/an ;
- Baisse du DFGe>30% en 4 mois sans cause évidente ;
- Hypertension résistante ;
- Hyperkaliémie persistante ;
- Doute étiologique.
Un adressage précoce améliore la qualité des soins et réduit la fréquence de démarrage de dialyse en urgence 1,2,6.
CE QUI CHANGE
Le RAC devient une cible
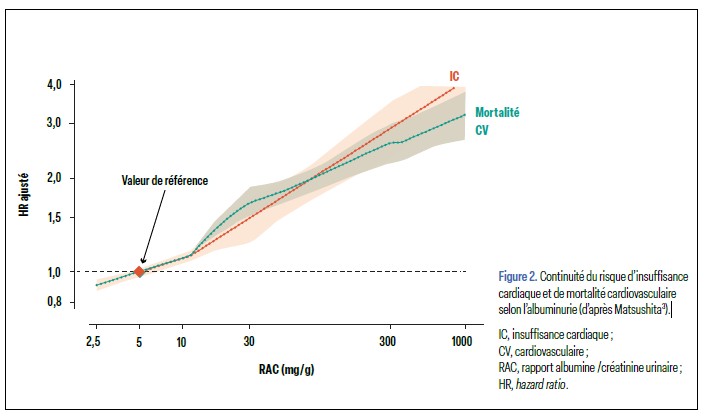
Le risque cardio-rénal augmente de façon continue avec le RAC, sans valeur seuil, ce qui justifie d'agir tôt et de ne pas négliger les valeurs dites «normales hautes»3-5 (Figure 2). Une réduction mesurable prédit une baisse proportionnelle du risque rénal et cardiovasculaire ; il faut viser l'albuminurie la plus basse possible. Les iSGLT2 et la finérénone s'additionnent aux IEC/ARA2 pour réduire le RAC et les événements cardiorénaux1,5.
L'abandon de la protéinurie
Le dosage de l'albuminurie et du RAC remplace celui de la protéinurie, car il est plus sensible et reproductible1,2. Ce virage progressif est rendu possible par le changement de nomenclature donnant au biologiste l'initiative de doser la créatinine urinaire lors d'une demande de protéinurie ou d'albuminurie7.
La stratification du risque (matrice GA) et le score de risque de progression rénale (KFRE) reposent sur les valeurs du RAC. De plus, certaines indications thérapeutiques (iSGLT2, finérénone) sont uniquement basées sur des valeurs d'albuminurie1,2.
Lecture standardisée
Les biologistes standardisent l'expression en mg/g et adjoignent des messages d'aide à la décision, ce qui rend le résultat immédiatement exploitable en consultation6.
CE QUE NOUS FERONS
Prescription groupée
Généraliser la prescription du «bilan rénal» standard qui combine systématiquement l'estimation du DFG et celle du RAC, pour éviter des demandes dissociées et incomplètes. Ceci se fait dans d'autres pays6.
Comptes rendus augmentés
Automatiser les signaux utiles dans les comptes rendus. Quand le DFGe est anormal, afficher « penser à mesurer le RAC ». Quand le RAC est ≥ 30 mg/g, rappeler de confirmer deux fois en 3-6 mois, de catégoriser A1-A3 et de situer la case de la matrice GA. Cette pratique est déjà expérimentée dans certaines régions6.
Parcours MG—biologie—néphrologie
Établir un canal d'avis rapide pour les patients avec un RAC≥300 mg/g ou un doublement du RAC2,6.
Suivi de trajectoire
Documenter la variation annuelle du RAC et améliorer la fréquence des contrôles guidée par la matrice GA1,2.
Conclusion
- CE QUE NOUS FAISONS: RAC premier matin en mg/g, confirmation si anomalie, décision croisée avec DFGe, adressage en cas d'albuminurie>300 mg/g (A3), DFGe < 45 ou déclin rapide..
- CE QUI CHANGE: le RAC devient une cible thérapeutique ; le traitement est IEC/ARA2 + iSGLT2 ± finérénone ; la protéinurie est abandonnée pour la décision.
- CE QUE NOUS FERONS:rappels automatiques labo, protocole pluriprofessionnel, maintien des traitements protecteurs avec surveillance de la kaliémie, suivi longitudinal du RAC.
Pr Thierry Hannedouche
Faculté de Médecine, Université de Strasbourg
Le Pr Thierry Hannedouche déclare avoir reçu des honoraires pour des présentations scientifiques par les laboratoires AstraZeneca et Fresenius Medical Care
Références
- Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2024 Clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int. 2024;105(4S):S117-S314.
- Guide du parcours de soins - Maladie rénale chronique de l'adulte (MRC) - Mis à jour le 17 nov. 2023. https://www.has-sante.fr/jcms/p_3288950/fr/guide-duparcours-de-soins-maladie-renale-chronique-de-l-adulte-mrc
- Matsushita K, Coresh J, Sang Y et coll. CKD Prognosis Consortium. Estimated glomerular filtration rate and albuminuria for prediction of cardiovascular outcomes: a collaborative meta-analysis of individual participant data. Lancet Diabetes Endocrinol. 2015; 3: 514-25.
- Grams ME, Coresh J, Matsushita K et coll. Estimated glomerular filtration rate, albuminuria, and adverse outcomes: an individual-participant data metaanalysis. JAMA. 2023; 330: 1266-1277
- Coresh J, Heerspink HJL, Sang Y et coll.; Chronic Kidney Disease Prognosis Consortium and Chronic Kidney Disease Epidemiology Collaboration. Change in albuminuria and subsequent risk of end-stage kidney disease : an individual participant-level consortium meta-analysis of observational studies. Lancet Diabetes Endocrinol. 2019;7(2):115-127.
- Hannedouche T, Rossignol P, Darmon P et coll. Early diagnosis of chronic kidney disease in patients with diabetes in France: multidisciplinary expert opinion, prevention value and practical recommendations. Postgrad Med. 2023; 135: 633-645
- Décision du 22 avril 2025 de l'UNCAM. NOR : TSSU2514781S. Journal Officiel du 23 mai 2025.
Abréviations
RAC : rapport albumine/créatinine urinaire ; CV : cardiovasculaire ; ARA2 : antagonistes des récepteurs de l'angiotensine II ; ARM : antagonistes des récepteurs minéralocorticoïdes ; DFGe : débit de filtration glomérulaire estimé ; HAS : Haute Autorité de Santé ; iSGLT2 : inhibiteurs du cotransporteur sodium glucose de type 2 ; IEC : inhibiteurs de l'enzyme de conversion ; IRCT : insuffisance rénale chronique terminale ; KDIGO : Kidney Disease Improving Global Outcomes ; KFRE : Kidney Failure Risk Equation ; MRC : maladie rénale chronique.


