La fibrillation atriale (FA) est l’arythmie cardiaque la plus fréquente. Elle touche environ 1% de la population française et sa prévalence augmente considérablement chez les sujets âgés. Pour les patients de plus de 80 ans, la prévalence est d’environ 10%1. De plus, 70% des patients qui font de la FA ont un âge compris entre 65 et 85 ans2.
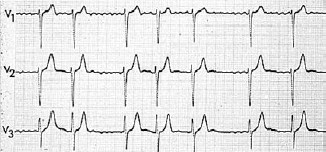
Figure 1 : Tracé ECG de fibrillation atriale avec rythme cardiaque irrégulier et trémulation de la ligne
La prise en charge de la fibrillation auriculaire repose sur deux traitements :
- Le traitement anti-arythmique
On distinguera les stratégies thérapeutiques visant à maintenir le rythme sinusal (RS) pour la FA paroxystique ou persistante, des stratégies visant à ralentir la fréquence cardiaque (FC) ventriculaire en laissant le patient en FA (FA permanente). Ces stratégies ont pour but de diminuer les symptômes des patients et d’éviter la survenue d’une insuffisance cardiaque, qui est favorisée par la perte de la systole atriale et une FC élevée.
- Le traitement anti-thrombotique
La survenue d’une FA favorise la survenue d’embolie artérielle systémique, notamment d’accident vasculaire cérébral (AVC), justifiant la mise sous anticoagulants au long cours. Cette indication est basée essentiellement sur le score de CHA2DS2VA qui sera calculé pour chaque patient.
Traitement anti-arythmique
On distinguera la prise en charge anti-arythmique au cours de la FA paroxystique, persistante ou permanente. Cet article est basé sur les dernières recommandations européennes publiées en 20243.
FA paroxystique
Les options possibles sont : l’utilisation de médicaments anti-arythmiques ou l’ablation de la FA.
Anti-arythmiques
Il existe plusieurs traitements anti-arythmiques pour le maintien en RS. En France, les traitements les plus couramment utilisés sont : le flécaïnide, le sotalol et l’amiodarone. D’une manière générale, l’amiodarone est plus efficace que le flécaïnide ou le sotalol, mais avec des effets secondaires plus importants. Par ailleurs, l’utilisation de l’amiodarone peut entraîner de nombreux effets secondaires possiblement responsables d’un arrêt du traitement : bradycardie, dysthyroïdie, toxicité pulmonaire, dépôt oculaire, perturbation hépatique ou atteinte neurologique. Ces effets secondaires sont le plus souvent cumulatifs dans le temps.
Le flécaïnide et le sotalol ont un index thérapeutique faible et peuvent entraîner des effets secondaires, notamment pro-arythmogènes. Le flécaïnide est principalement contre-indiqué en cas d’insuffisance cardiaque ou de cardiopathie ischémique.
Ce traitement peut élargir les QRS, avec un élargissement qui doit rester inférieur à 150% de la largeur du QRS initial. Le sotalol allonge l’intervalle QT et le QTc doit être suivi régulièrement et rester <520ms. Ce traitement est aussi contre-indiqué en cas d’insuffisance cardiaque.
Ablation de la FA
Il s’agit d’une technique percutanée invasive qui s’est développée de manière très importante ces 20 dernières années. Elle consiste à éliminer les foyers arythmogènes responsables de la FA.
Pour la FA paroxystique, ces foyers sont situés autour des veines pulmonaires. Pour la FA persistante, il est souvent nécessaire de réaliser des lésions complémentaires soit à type de lignes dans les oreillettes, soit de traiter des zones focales. Le taux de succès de cette procédure est d’environ 70-80% en cas de FA paroxystique et 50-60% en cas de FA persistante. Il est possible, en cas de récidive, de refaire une nouvelle procédure. Les risques de cette technique sont l’AVC, la tamponnade et la fistule atrio-oesophagienne qui a un pronostic très sombre. Le taux global de complications est de 2 à 3%.
D’une manière générale, les différentes options thérapeutiques doivent en premier lieu être discutées avec le patient. Le rapport bénéfice/risque de chacune de ces stratégies doit être expliqué au patient et la décision thérapeutique doit être éclairée et acceptée par le patient (Figure 2). Concernant l’ablation de FA, même si cette technique s’est considérablement améliorée ces dernières années avec une amélioration du taux de succès et une diminution des complications, elle reste une intervention invasive avec des complications potentiellement graves.
Un autre paramètre important est l’état physiologique du patient. Plus le patient sera jeune avec moins de comorbidités, plus les stratégies essaieront de «guérir» le patient de cette pathologie, en proposant une ablation FA précocement : soit après l’échec d’un traitement médicamenteux (souvent le flécaïnide), soit d’emblée. Par ailleurs, les patients jeunes sont souvent peu enclins à prendre des traitements anti-arythmiques de manière quotidienne et potentiellement à vie, ce qui les oriente rapidement vers une stratégie d’ablation de FA. À l’inverse plus les patients seront âgés, avec des comorbidités, moins on proposera la réalisation de gestes invasifs comme l’ablation de FA ou le choc électrique externe (CEE).
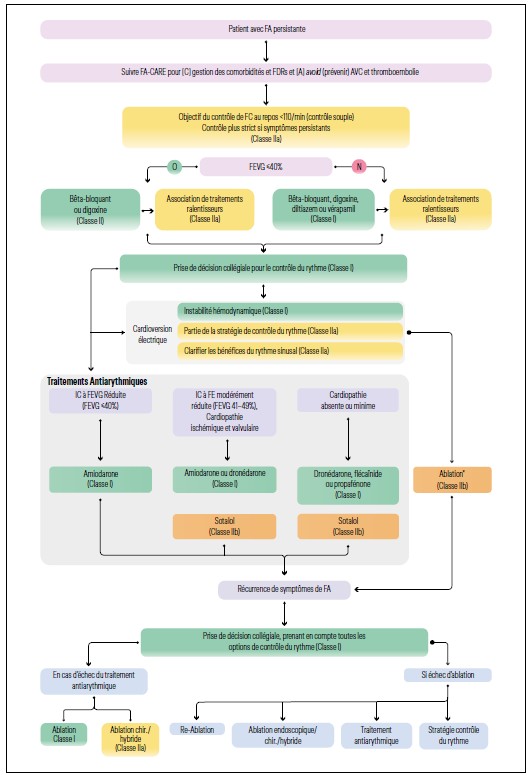
Figure 2 : Arbre diagnostique pour le traitement anti-arythmique de la FA paroxystique.
FA persistante
Pour la FA persistante, une cardioversion médicamenteuse et/ou électrique sera nécessaire pour remettre le patient en RS. Pour remettre un patient en RS, on débute en général par une tentative de cardioversion médicamenteuse consistant en l’administration d’une dose de charge d’amiodarone, soit per os soit IV. Si ce traitement ne permet pas le retour en RS, on pratiquera un choc électrique externe (CEE). Il faudra alors maintenir le traitement anti-arythmique pour augmenter le taux de succès immédiat du CEE qui est d’environ 95 % et réduire le risque de récidive à distance du choc.
Une fois le patient revenu en RS, il faudra se poser la question du maintien en RS et la stratégie thérapeutique à adopter, qui est basée sur les mêmes principes que le traitement de la FA paroxystique (Figure 3).
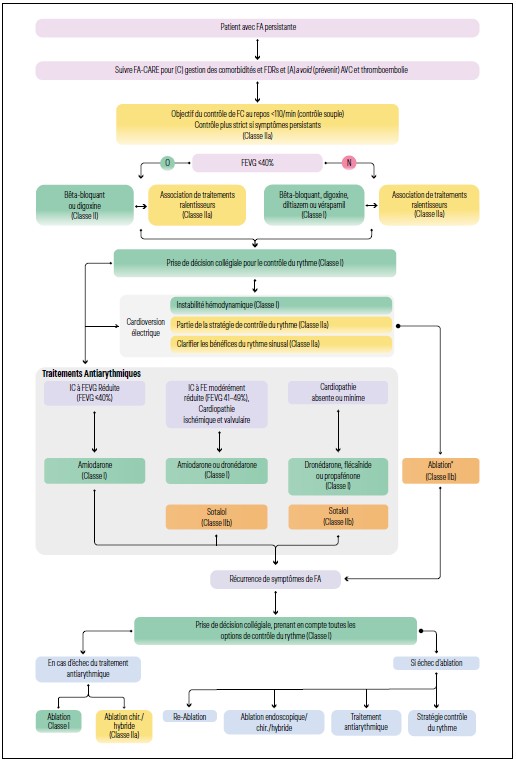
Figure 3 : Arbre diagnostique pour le traitement anti-arythmique de la FA persistante.
FA permanente
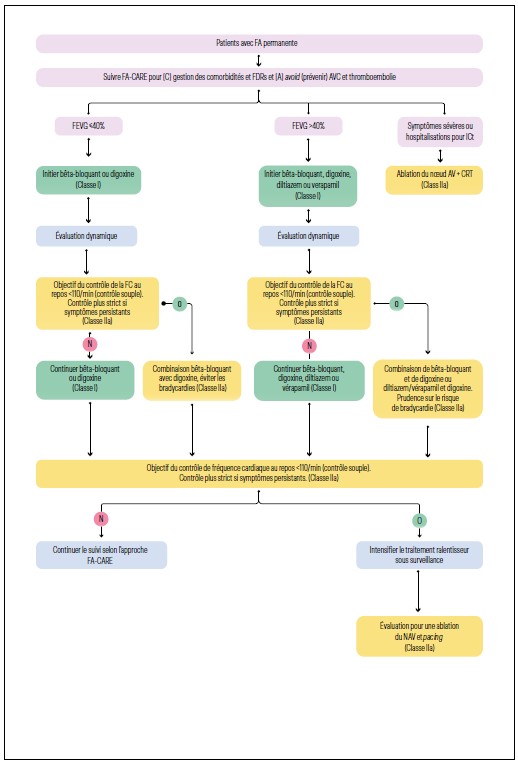
Dans ce cas, il est décidé de laisser le patient en FA. Il s’agit souvent de personnes âgées, pauci-symptomatiques avec de nombreuses comorbidités. L’autre situation correspond à des patients pour lesquels plusieurs tentatives de maintien en RS par médicaments (souvent amiodarone), ablation de FA et/ou CEE itératifs ont fini par un échec. Il s’agit donc d’une stratégie de contrôle de la FC.
Les traitements les plus fréquemment utilisés pour ralentir la FA sont les bêtabloquants, les inhibiteurs calciques bradycardisants et la digoxine.
La FC cible est une fréquence inférieure à 80 au repos et 110 bpm à l’effort. En cas de persistance des symptômes, la cible de FC peut être plus stricte au cas par cas avec un monitoring ECG afin de limiter la survenue de toute bradycardie sévère chez des patients fragiles.
Les bêtabloquants sont les plus efficaces pour atteindre cet objectif. Les inhibiteurs calciques bradycardisants (vérapamil et diltiazem) peuvent être utilisés en alternative, en général lorsqu’il existe une contre-indication aux bêtabloquants (par exemple, asthme ou syndrome de Raynaud).
Enfin, la digoxine doit être utilisée avec précaution surtout chez les patients avec insuffisance rénale, car la marge thérapeutique est faible et la toxicité potentielle du médicament est importante. La seule indication à retenir est celle de l’insuffisance cardiaque aiguë associée à une FA rapide.
Lorsque les symptômes (type insuffisance cardiaque, palpitations, malaises) sont mal contrôlés avec ces médicaments, on peut proposer l’implantation d’un pace-maker (PM) puis l’ablation du nœud auriculo-ventriculaire (NAV) pour obtenir un bloc auriculo-ventriculaire complet (Figure 4).
Figure 4 : Arbre diagnostique proposé pour le contrôle de la fréquence cardiaque dans la FA permanente.
Prévention thromboembolique au cours de la FA
La prévention thromboembolique repose sur deux stratégies thérapeutiques : le traitement anticoagulant, représenté essentiellement par les AOD, et la fermeture percutanée de l’auricule gauche.
Traitements anticoagulants
Depuis un peu plus d’une décennie, les anticoagulants oraux directs (AOD) sont utilisés en alternative aux antivitamines K (AVK) pour traiter la FA. Les AOD sont maintenant plus prescrits que les AVK du fait de leur facilité de prescription et de suivi. Malgré ces avancées, cela reste un traitement anticoagulant qui comporte des risques d’hémorragie, parfois très grave, ce qui nécessite des précautions d’emploi et un suivi régulier du patient.
On utilise actuellement en France trois AOD : un antithrombine, le dabigatran (Pradaxa), et deux anti-Xa, l’apixaban (Eliquis) et le rivaroxaban (Xarelto). Ces traitements sont utilisés par voie orale, en une prise pour le rivaroxaban et 2 prises pour le dabigatran et l’apixaban. Enfin, un avantage majeur de ces produits est l’absence de nécessité de suivi par des tests d’hémostase dans le cadre du traitement courant.
Les AOD ont montré une réduction des hémorragies graves, notamment cérébrales (réduction d’environ 50 % du risque d’hémorragie intracrânienne) par rapport aux AVK4.
Indications
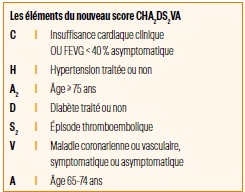
L’indication d’un traitement anticoagulant au long cours est guidée par le calcul du score CHA2DS2VA, qui représente le risque thromboembolique du patient (Figure 5). Si ce score est de 0, il n’y a pas d’indication à un traitement anticoagulant au long cours. S’il est à 1, le traitement anticoagulant est plutôt recommandé (classe IIa). Enfin, s’il est au-dessus de 2, il est formellement indiqué au long cours3.
Figure 5 : Items présents dans le score de CHA2DS2VA.
Le risque hémorragique du patient est évalué en notifiant les facteurs de risque d’hémorragie modifiables comme l’HTA ou la prise de médicaments associés comme les antiagrégants plaquettaires ou les AINS et les non modifiables comme l’âge, les antécédents d’AVC, l’insuffisance rénale ou hépatique. L’utilisation de scores spécifiques n’est plus recommandée.
La seule indication restant aux AVK dans un contexte de FA est un patient porteur d’une prothèse cardiaque mécanique ou d’une sténose mitrale rhumatismale (FA valvulaire)3.
Par ailleurs, chez un patient déjà traité par des AVK et des INR stables, il est conseillé de poursuivre le traitement par AVK.
Effets secondaires
L’hémorragie mineure et surtout majeure est le risque le plus important avec ce type de traitement. Des effets secondaires plus rares ont été décrits : allergie, hépatite ou alopécie.
Contre-indications
Ces traitements sont contre-indiqués chez des patients présentant une hémorragie non maîtrisée, une allergie déjà connue à ce type de produit ou une insuffisance hépatique sévère.
Interactions médicamenteuses
Des interactions médicamenteuses significatives ont été décrites avec les inhibiteurs de la P-gp (antiprotéases, antifongiques) ou des inducteurs de la P-gp (rifampicine, carbamazépine ou phénytoïne). Une interaction médicamenteuse spécifique mérite d’être signalée : il s‘agit de celle entre le vérapamil (Isoptine) et le dabigatran ; cette association médicamenteuse doit conduire à une réduction de dose du dabigatran à 110 mg x 2/j quelle que soit la fonction rénale. Enfin, une surveillance particulière est également nécessaire en cas d’association avec l’amiodarone du fait d’un surrisque hémorragique potentiel, même si une adaptation de dose de dabigatran n’est pas systématique.
Fermeture percutanée de l’auricule gauche
La fermeture percutanée de l’auricule gauche est une technique interventionnelle visant à fermer l’auricule gauche, qui est la zone dans l’oreillette gauche où se forme le thrombus au cours de la FA (Figure 6).
Figure 6 : Schéma montrant les deux types de prothèse disponibles en France pour fermer l’auricule gauche. A. Amplatzer (Abbott). B. Watchman (Boston Dynamics). DR.
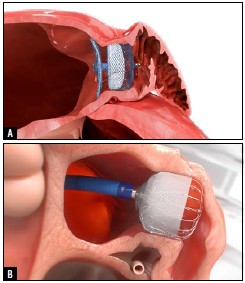
En fermant cet appendice, on réduit le risque d’AVC. Ceci a été montré dans de nombreuses études. Ainsi, il est possible actuellement de proposer cette thérapeutique à des patients ayant une indication théorique aux anticoagulants au long cours, mais présentant une contre-indication aux anticoagulants. Son indication nécessite une réunion multidisciplinaire, incluant au moins un cardiologue et le spécialiste de l’organe présentant le saignement (neurologue, gastro-entérologue ou urologue). Les risques de cette intervention sont la survenue d’un AVC, une tamponnade ou une embolisation de la prothèse. Le taux global de complications est d’environ 2-3%. Par la suite, un suivi par imagerie cardiaque par scanner est nécessaire pour dépister la présence d’une fuite para-prothétique ou d’un thrombus sur prothèse (2-3% des cas).
Enfin, un traitement anticoagulant ou antiagrégant reste recommandé pendant au moins 1-2 mois après l’intervention pour diminuer le risque de thrombose sur prothèse. Parfois, aucun traitement antithrombotique n’est possible. De nombreuses études sont en cours pour mieux préciser l’efficacité et la tolérance de cette procédure dans plusieurs indications.
Pr Nicolas Lellouche
Unité de rythmologie, Service de Cardiologie,
CHU Henri Mondor de Créteil, APHP
L’auteur déclare ne pas avoir de lien d’intérêt pour cet article.
Cet article est le second d'une série de quatre articles rédigés par le Pr Nicolas Lellouche à la demande de l'ARMP sur les « Troubles du rythme et médecine générale »
Références
- Go AS, Hylek EM, Phillips KA et coll. Prevalence of diagnosed atrial fibrillation in adults: National implications for rhythm management and stroke prevention: The anticoagulation and risk factors in atrial fibrillation (ATRIA) study. JAMA, 2001; 285: 2370–2375.
- Kistler P, Sanders P, Fynn S et coll. Electrophysiologic and electro-anatomic changes in the human atrium associated with age. J Am Coll Cardiol, 2004; 44: 109–116.
- Van Gelder IC, Rienstra M, Bunting KV et coll; ESC Scientific Document Group. 2024 ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J, 2024; 45: 3314–3414.
- Ruff CT, Giugliano RP, Braunwald E et coll. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a metaanalysis of randomised trials. Lancet, 2014; 383: 955–62.